การเปลี่ยนแปลงแบบอะเดียแบติกระหว่างสองสถานะในก๊าซไม่ใช่หนึ่งในกระบวนการไอโซโพรเซส อย่างไรก็ตาม มันมีบทบาทสำคัญในกระบวนการทางเทคโนโลยีต่างๆ ไม่เพียงเท่านั้น แต่ยังรวมถึงในธรรมชาติด้วย ในบทความนี้ เราจะพิจารณาว่ากระบวนการนี้คืออะไร และยังให้สมการอะเดียแบติกสำหรับก๊าซในอุดมคติด้วย
สรุปแก๊สในอุดมคติ
ก๊าซในอุดมคติคือก๊าซที่ไม่มีปฏิสัมพันธ์ระหว่างอนุภาคของมัน และมีขนาดเท่ากับศูนย์ แน่นอนว่าตามธรรมชาติแล้ว ไม่มีก๊าซในอุดมคติร้อยเปอร์เซ็นต์ เนื่องจากพวกมันทั้งหมดประกอบด้วยโมเลกุลและอะตอมของขนาด ซึ่งจะมีปฏิสัมพันธ์ซึ่งกันและกัน อย่างน้อยก็ด้วยความช่วยเหลือของกองกำลังแวนเดอร์วาลส์ อย่างไรก็ตาม แบบจำลองที่อธิบายไว้มักจะดำเนินการด้วยความแม่นยำเพียงพอสำหรับการแก้ปัญหาในทางปฏิบัติสำหรับก๊าซจริงจำนวนมาก
สมการหลักของก๊าซในอุดมคติคือกฎของแคลเปย์รอน-เมนเดเลเยฟ มันเขียนในรูปแบบต่อไปนี้:
PV=nRT.
สมการนี้กำหนดสัดส่วนโดยตรงระหว่างผลิตภัณฑ์ความดัน P บนปริมาตร V และปริมาณของสาร n ต่ออุณหภูมิสัมบูรณ์ T ค่าของ R คือค่าคงที่ของแก๊สซึ่งทำหน้าที่เป็นตัวประกอบสัดส่วน
กระบวนการอะเดียแบติกคืออะไร
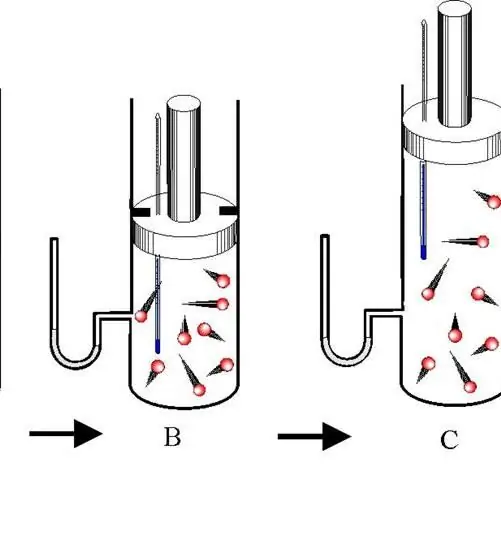
กระบวนการอะเดียแบติกคือการเปลี่ยนแปลงระหว่างสถานะของระบบแก๊สซึ่งไม่มีการแลกเปลี่ยนพลังงานกับสิ่งแวดล้อม ในกรณีนี้ ลักษณะทางอุณหพลศาสตร์ทั้งสามของระบบ (P, V, T) จะเปลี่ยนไป และปริมาณของสาร n จะคงที่
แยกแยะระหว่างการขยายตัวและการหดตัวของอะเดียแบติก ทั้งสองกระบวนการเกิดขึ้นเนื่องจากพลังงานภายในของระบบเท่านั้น จากการขยายตัวทำให้ความดันและโดยเฉพาะอย่างยิ่งอุณหภูมิของระบบลดลงอย่างมาก ในทางกลับกัน การกดทับแบบอะเดียแบติกส่งผลให้อุณหภูมิและความดันเพิ่มขึ้นในเชิงบวก
เพื่อป้องกันการแลกเปลี่ยนความร้อนระหว่างสิ่งแวดล้อมและระบบ หลังต้องมีผนังฉนวนกันความร้อน นอกจากนี้ การลดระยะเวลาดำเนินการยังช่วยลดการไหลของความร้อนเข้าและออกจากระบบได้อย่างมาก
สมการปัวซองสำหรับกระบวนการอะเดียแบติก

กฎข้อที่หนึ่งของอุณหพลศาสตร์เขียนดังนี้:
Q=ΔU + A.
กล่าวอีกนัยหนึ่ง ความร้อน Q ที่สื่อสารกับระบบถูกใช้เพื่อทำงาน A โดยระบบ และเพิ่มพลังงานภายใน ΔU ในการเขียนสมการอะเดียแบติก ควรใส่ Q=0 ซึ่งสอดคล้องกับคำจำกัดความของกระบวนการที่กำลังศึกษา เราได้:
ΔU=-A.
ด้วยไอโซโคริกในก๊าซอุดมคติ ความร้อนทั้งหมดจะไปเพิ่มพลังงานภายใน ข้อเท็จจริงนี้ทำให้เราเขียนความเท่าเทียมกันได้:
ΔU=CVΔT.
โดยที่ CV คือความจุความร้อนไอโซโคริก ในทางกลับกัน งาน A คำนวณได้ดังนี้
A=PdV.
ที่ dV คือการเปลี่ยนแปลงปริมาณเล็กน้อย
นอกเหนือจากสมการ Clapeyron-Mendeleev แล้ว สมการต่อไปนี้ถือเป็นก๊าซในอุดมคติ:
CP- CV=R.
โดยที่ CP คือความจุความร้อนไอโซบาริก ซึ่งมากกว่าความจุไอโซโคริกเสมอ เนื่องจากจะพิจารณาการสูญเสียก๊าซอันเนื่องมาจากการขยายตัว
วิเคราะห์สมการที่เขียนด้านบนและรวมอุณหภูมิและปริมาตร เรามาถึงสมการอะเดียแบติกต่อไปนี้:
TVγ-1=const.
ที่นี่ γ คือดัชนีอะเดียแบติก เท่ากับอัตราส่วนของความจุความร้อนไอโซบาริกต่อไอโซโคริก ความเท่าเทียมกันนี้เรียกว่าสมการปัวซองสำหรับกระบวนการอะเดียแบติก เมื่อใช้กฎ Clapeyron-Mendeleev คุณสามารถเขียนนิพจน์ที่คล้ายกันอีกสองนิพจน์ โดยใช้พารามิเตอร์ P-T และ P-V เท่านั้น:
TPγ/(γ-1)=const;
PVγ=const.
กราฟอะเดียแบติกสามารถกำหนดได้หลายแกน ด้านล่างแสดงเป็นแกน P-V
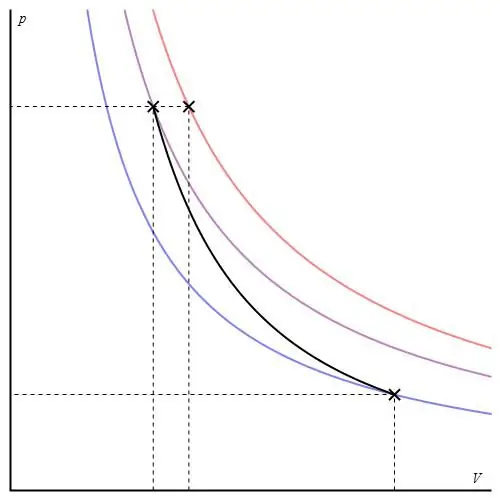
เส้นสีบนกราฟสอดคล้องกับไอโซเทอร์ม ส่วนโค้งสีดำคืออะเดียแบท ดังจะเห็นได้ว่า อะเดียบัตมีพฤติกรรมรุนแรงกว่าไอโซเทอร์มใดๆ ข้อเท็จจริงนี้อธิบายได้ง่าย: สำหรับไอโซเทอร์ม ความดันจะเปลี่ยนกลับตามสัดส่วนของปริมาตร แต่สำหรับไอโซบาธ ความดันจะเปลี่ยนเร็วขึ้น เนื่องจากเลขชี้กำลังคือ γ>1 สำหรับระบบแก๊สใดๆ
ตัวอย่างปัญหา
ในธรรมชาติ ในพื้นที่ภูเขา เมื่อมวลอากาศเคลื่อนตัวขึ้นไปบนทางลาด แรงดันจะลดลง ปริมาณอากาศจะเพิ่มขึ้นและเย็นลง กระบวนการอะเดียแบติกนี้ช่วยลดจุดน้ำค้างและทำให้เกิดฝนที่เป็นของเหลวและของแข็ง

เสนอให้แก้ปัญหาต่อไปนี้: ในกระบวนการยกมวลอากาศตามแนวลาดชันของภูเขา ความดันลดลง 30% เมื่อเทียบกับแรงดันที่เท้า อุณหภูมิเท่าไหร่ถ้าเท้าเป็น 25 oC?
ในการแก้ปัญหา ใช้สมการอะเดียแบติกต่อไปนี้:
TPγ/(γ-1)=const.
เขียนในแบบฟอร์มนี้ดีกว่า:
T2/T1=(P2/P 1)(γ-1)/γ.
ถ้า P1 ถูกนำมาเป็น 1 บรรยากาศ จากนั้น P2 จะเท่ากับ 0.7 บรรยากาศ สำหรับอากาศ ดัชนีอะเดียแบติกคือ 1.4 เนื่องจากถือได้ว่าเป็นก๊าซอุดมคติของไดอะตอม ค่าอุณหภูมิของ T1 คือ 298.15 K. แทนที่ตัวเลขทั้งหมดเหล่านี้ลงในนิพจน์ด้านบน เราจะได้ T2=269.26 K ซึ่งสอดคล้องกับ - 3, 9 oC.






